キーワード:レギュラトリーサイエンス、医薬品、医療機器
 大学の自由な風土や研究者の発想から多くの画期的な新薬や治療機器や革新的なシーズが生み出されています。こういった世相を追い風に大学の研究成果に注目が集まってきていますが、大学から企業への技術移転はあまり進んでいないのが実情です。技術移転が進まない原因の一つが、医薬品・医療機器の承認審査に必要となる厳しい安全性・有効性試験です。この規制は予想外の副作用を避けるために整備されているものですが、この試験を実施するには多額の費用を必要となります。リサーチユニット「レギュラトリーサイエンス」では、大 学の研究成果を迅速に社会へ適応させていくために重要な鍵となる2つの立場、自由と規制の橋渡しに挑戦しています。
大学の自由な風土や研究者の発想から多くの画期的な新薬や治療機器や革新的なシーズが生み出されています。こういった世相を追い風に大学の研究成果に注目が集まってきていますが、大学から企業への技術移転はあまり進んでいないのが実情です。技術移転が進まない原因の一つが、医薬品・医療機器の承認審査に必要となる厳しい安全性・有効性試験です。この規制は予想外の副作用を避けるために整備されているものですが、この試験を実施するには多額の費用を必要となります。リサーチユニット「レギュラトリーサイエンス」では、大 学の研究成果を迅速に社会へ適応させていくために重要な鍵となる2つの立場、自由と規制の橋渡しに挑戦しています。
医薬品・医療機器開発を促進するために大学ができること
レギュラトリーサイエンス*1とは「根拠に基づく的確な予測・評価・判断を行い、科学技術の成果を人と社会との調和の上で最も望ましい姿に調整するための科学」と定義されています。これは、大学での研究成果を医薬品・医療機器などに発展させていく際には、とくに重要な考え方になります。なぜかというと、人体に直接作用するような医薬品・医療機器には、予測できないリスクを避けるために厚生労働省と医薬品医療機器総合機構(PMDA)により非常に厳しい規制がかけられているからです。私たちはこの規制を遵守しつつ大学における研究の成果である革新的シーズの技術移転を促進させるために活動中です。私たちは、臨床で効果があることを示すのが一番であり、非臨床の有効性の試験こそ、大学でやるべき内容だと思っています(図1)。
*1 レギュラトリーサイエンス:医薬品食品衛生研究所の内山充氏が提唱した概念。第4期科学技術基本計画では「科学技術の成果を人と社会に役立てることを目的に、根拠に基づく的確な予測、評価、判断を行い、科学技術の成果を人と社会との調和の上で最も望ましい姿に調整するための科学」と定義されている。

いいものを作りたい研究者と、品質・安全性を重視する企業の間を埋め、技術移転を加速させる
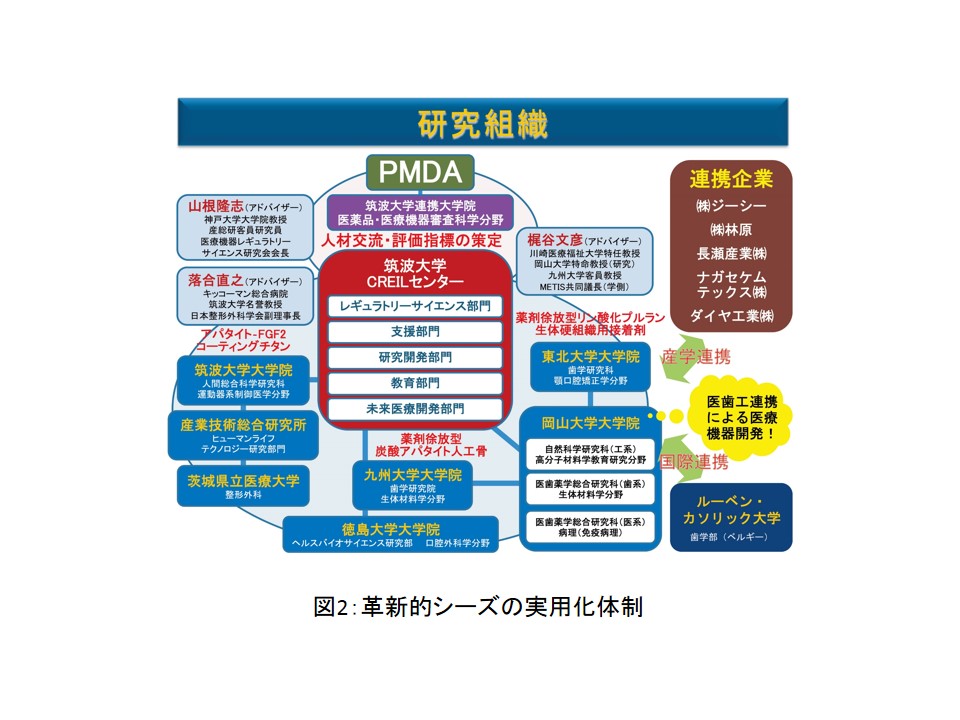
「薬をつくろう」「医療機器をつくろう」と思って研究をしても、なかなかできるものではありません。やはり大学の基礎研究の段階では、研究者の思うことを突き詰め、薬になる可能性がでてきたところで、ほんの少しだけ研究のなかに、レギュラトリーサイエンスの観点を入れていくのが良いと思っています。薬品や 医療機器の開発では研究とは異なる視点が必要な場合があります。ある時点で一旦研究を止めないと開発には進めません。常にいいものを作りたいと思っている研究者と、品質・安全性を重視する企業の間を埋めることで、より短期間な開発が可能になる、そんな体制を構築しているところです(図2)。
社会への貢献・実績
● リン酸化プルランを用いた世界初の多目的接着性人工骨の開発
● 革新的硬組織再生・再建システム創製
(取材:平成25年6月17日)
Accelerate Technology Transfer by Relaxing the Boundary between Freedom and Regulations
Key words: regulatory science, pharmaceuticals, medical devices
http://www.md.tsukuba.ac.jp/CREIL/en/index.html
Various new drugs, medical devices, and innovative seeds have been produced based on ideas from free thinking researchers at universities. This has drawn attention to research achievements of universities. However, technology transfer from universities to companies remains delayed. This delayed technology transfer is partially explained by the strict safety and efficacy tests required for the approval of  pharmaceuticals and medical devices. These regulations were set to avoid unexpected adverse effects. However, significant costs must be met to implement the tests. Our unit is trying to bridge the gap between freedom and regulation, two attitudes critical for rapidly utilizing the research achievements of universities to benefit society.
pharmaceuticals and medical devices. These regulations were set to avoid unexpected adverse effects. However, significant costs must be met to implement the tests. Our unit is trying to bridge the gap between freedom and regulation, two attitudes critical for rapidly utilizing the research achievements of universities to benefit society.
What can universities do to facilitate the development of pharmaceuticals and medical devices?
Regulatory science*1 is defined as “science to make accurate prediction, evaluation, and judgment based on evidence and benefit most from scientific and technological achievements to promote harmony between human life and society.” This is critical for utilizing the research achievements of universities for the development of pharmaceuticals and medical devices. This is because strict regulations are imposed by the Ministry of Health, Labour and Welfare and the Pharmaceuticals and Medical Devices Agency (PMDA) on pharmaceuticals and medical devices that act directly on the human body, in order to avoid their unpredictable risks. Our unit is trying to facilitate the technology transfer of innovative seeds as research achievements from universities, while complying with these regulations. We consider that the most important objective is to demonstrate the clinical effects, and that non-clinical efficacy tests should be conducted by universities (Figure 1).
Accelerate technology transfer for the development of new drugs and medical devices
We face difficulties filling the gap between researchers who focus on their research achievements and companies that focus on quality and safety. At the stage of basic research at universities, researchers should focus on their investigations, and regulatory science should be gradually considered when seeds are obtained. Pharmaceuticals and medical devices should be developed from viewpoints different from those of research. Research should be discontinued at a certain stage to proceed to development. We are trying to establish a system by which the gap between researchers who always focus on their research achievements and companies that focus on quality and safety is filled to facilitate the development of new drugs and medical devices (Figure 2).
*1Regulatory science: A concept proposed by Mitsuru Uchiyama of the National Institute of Health Sciences. According to the 4th Science and Technology Basic Plan, regulatory science is defined as “science to make accurate prediction, evaluation, and judgment based on evidence and benefit most from scientific and technological achievements to promote harmony between human life and society, in order to utilize scientific and technological achievements for human life and society.”
Social contributions and achievements
● Development of world’s first multi-purpose adhesive artificial bone using phosphorylated pullulan
● Creation of innovative hard tissue regeneration and reconstruction systems


